Acide perfluorooctanesulfonique
L'acide perfluorooctanesulfonique (PFOS), dont la base conjuguée est l'anion perfluorooctanesulfonate, est un sulfonate d'alkyle perfluoré utilisé comme tensioactif fluoré de formule brute C8F17SO3H. C'est un perturbateur endocrinien et un polluant inscrit à l'Annexe B de la Convention de Stockholm sur les polluants organiques persistants.
| Acide perfluorooctanesulfonique | |||
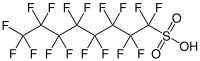
| |||
 Anion perfluorooctanesulfonate |
|||
| Identification | |||
|---|---|---|---|
| Nom UICPA | acide 1,1,2,2,3,3,4,4,5,5,6,6,7,7,8,8,8-heptadécafluorooctane-1-sulfonique | ||
| Synonymes |
acide perfluorooctylsulfonique |
||
| No CAS | (molécule neutre) (anion sulfonate) |
||
| No ECHA | 100.015.618 | ||
| No CE | 217-179-8 (molécule neutre) | ||
| PubChem | 74483 | ||
| ChEBI | 39421 | ||
| SMILES | |||
| InChI | |||
| Propriétés chimiques | |||
| Formule | C8HF17O3S [Isomères] |
||
| Masse molaire[1] | 500,13 ± 0,012 g/mol C 19,21 %, H 0,2 %, F 64,58 %, O 9,6 %, S 6,41 %, |
||
| Précautions | |||
| SGH[2],[3] | |||
| H302, H332, H351, H360D, H362, H372, H411, P201, P263, P273, P281 et P308+P313 |
|||
| Transport[3] | |||
|
|||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
Usages
modifierIl dérive notamment du perfluorooctanesulfonamide C8F17SO2NH2 (PFOSA) et a constitué jusqu'au début du siècle l'ingrédient essentiel du traitement Scotchgard mis au point par la société 3M pour l'imperméabilisation des tissus, du mobilier et des tapis[4]. Il a également été utilisé pour traiter les papiers à contact alimentaire contre les taches d'eau et de graisse[5], ainsi que pour diverses autres applications grand public[6].
Production
modifierLa préparation des PFOS s'effectue par fluoration électrochimique du chlorure d'octanesulfonyle dans le fluorure d'hydrogène anhydre. Il en résulte trois quarts de fluorure de perfluorooctanesulfonyle linéaire et un quart de fluorure de perfluorooctanesulfonyle ramifié.
Le PFOS est obtenu par hydrolyse du fluorure de perfluorooctanesulfonyle[7],[8].
Outre l'isomère linéaire, il existe 88 isomères de constitution ramifiés possibles du PFOS[9].
Propriétés
modifierC'est une molécule amphiphile, avec une chaîne latérale à la fois hydrophobe et lipophobe, et un groupe sulfonate ou acide sulfonique terminal hydrophile. Il est particulièrement stable en raison de la force des liaisons carbone-fluor. C'est un tensioactif plus puissant que ceux à base d'hydrocarbures.
Réglementation globale
modifierEn 2009, PFOS, ses sels et fluorure de perfluorooctanesulfonyle ont été classés parmi les POPs (polluants organiques persistants), au titre de la Convention de Stockholm en raison de leur nature omniprésente, persistante, bioaccumulable et toxique[10].
Articles connexes
modifier- L'acide perfluorooctanesulfonique est utilisé dans le Skydrol.
Notes et références
modifier- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée « Perfluorooctane sulfonic acid » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 15 mars 2013 (JavaScript nécessaire)
- Fiche Sigma-Aldrich du composé Acide perfluorooctanesulfonique ~ 40 % dans H2O, consultée le 15 mars 2013.
- (en) Bryan Boulanger, John D. Vargo, Jerald L. Schnoor et Keri C. Hornbuckle, « Evaluation of Perfluorooctane Surfactants in a Wastewater Treatment System and in a Commercial Surface Protection Product », Environmental Science and Technology, vol. 39, no 15, , p. 5524-5530 (lire en ligne) DOI 10.1021/es050213u
- (en) Hermann Fromme, Sheryl A. Tittlemier, Wolfgang Völkel, Michael Wilhelm et Dorothee Twardella, « Perfluorinated compounds – Exposure assessment for the general population in western countries », International Journal of Hygiene and Environmental Health, vol. 212, no 3, , p. 239-270 (lire en ligne) DOI 10.1016/j.ijheh.2008.04.007
- (en) Geary W. Olsen, Timothy R. Church, Eric B. Larson, Gerald van Belle, James K. Lundberg, Kristen J. Hansen, Jean M. Burris, Jeffrey H. Mandel et Larry R. Zobel, « Serum concentrations of perfluorooctanesulfonate and other fluorochemicals in an elderly population from Seattle, Washington », Chemosphere, vol. 54, no 11, , p. 1599-1611 (PMID 14675839, DOI 10.1016/j.chemosphere.2003.09.025, lire en ligne)
- (en) Robert C Buck, James Franklin, Urs Berger et Jason M Conder, « Perfluoroalkyl and polyfluoroalkyl substances in the environment: Terminology, classification, and origins », Integrated Environmental Assessment and Management, vol. 7, no 4, , p. 513–541 (PMID 21793199, PMCID PMC3214619, DOI 10.1002/ieam.258, lire en ligne)
- (en) Hans-Joachim Lehmler, « Synthesis of environmentally relevant fluorinated surfactants—a review », Chemosphere, vol. 58, no 11, , p. 1471–1496 (DOI 10.1016/j.chemosphere.2004.11.078, lire en ligne)
- (en) Sierra Rayne, Kaya Forest et Ken J. Friesen, « Congener-specific numbering systems for the environmentally relevant C4 through C8 perfluorinated homologue groups of alkyl sulfonates, carboxylates, telomer alcohols, olefins, and acids, and their derivatives », Journal of Environmental Science and Health, Part A, vol. 43, no 12, , p. 1391–1401 (DOI 10.1080/10934520802232030)
- (en-GB) « Information on the 16 chemicals added to the Stockholm Convention – Perfluorooctane sulfonic acid (PFOS), its salts and perfluorooctane sulfonyl fluoride (PFOS-F) », sur pops.int (consulté le )




