Chlorure d'hexaamminenickel(II)
composé chimique
Le chlorure d'hexaamminenickel(II) est un sel de complexe métallique de formule chimique [Ni(NH3)6]Cl2. Ce chlorure de l'hexaammine de nickel à l'état d'oxydation +2 est un solide cristallisé paramagnétique d'un bleu intense. Les six ligands ammoniac NH3 du cation [Ni(NH3)6]2+ sont coordonnés autour du nickel selon une géométrie octaédrique[3].
-
Poudre de [Ni(NH3)6]Cl2.
| Chlorure d'hexaamminenickel(II) | |
| |
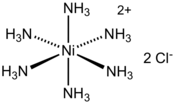
| Structure du chlorure d'hexaamminenickel(II) | |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.149.740 |
| No CE | 620-832-3 |
| PubChem | 22221640 |
| SMILES | |
| InChI | |
| Apparence | solide cristallisé d'un bleu intense |
| Propriétés chimiques | |
| Formule | H18Cl2N6Ni |
| Masse molaire[1] | 231,783 ± 0,007 g/mol H 7,83 %, Cl 30,59 %, N 36,26 %, Ni 25,32 %, |
| Précautions | |
| SGH[2] | |
| H302, H312, H317, H332, H334 et H350 |
|
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
On peut l'obtenir en traitant une solution aqueuse de chlorure de nickel(II) NiCl2 avec de l'ammoniac NH3. C'est une source moléculaire de nickel(II) anhydre en synthèse chimique[4].
Notes et références
modifier- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Hexaamminenickel(II) chloride », sur echa.europa.eu, ECHA (consulté le ).
- (de) Ralf Eßmann, Guido Kreiner, Anke Niemann, Dirk Rechenbach, Axel Schmieding, Thomas Sichla, Uwe Zachwieja et Herbert Jacobs, « Isotype Strukturen einiger Hexaamminmetall(II)-halogenide von 3d-Metallen: [V(NH3)6]I2, [Cr(NH3)6]I2, [Mn(NH3)6]Cl2, [Fe(NH3)6]Cl2, [Fe(NH3)6]Br2, [Co(NH3)6]Br2 und [Ni(NH3)6]Cl2 », Zeitschrift für anorganische une allgemeine Chemie, vol. 622, no 7, , p. 1161-1166 (DOI 10.1002/zaac.19966220709, lire en ligne).
- (en) G. S. Girolami, T. B. Rauchfuss et R. J. Angelici, Synthesis and Technique in Inorganic Chemistry, University Science Books, 1999. (ISBN 0-935702482)
![Poudre de [Ni(NH3)6]Cl2.](http://upload.wikimedia.org/wikipedia/commons/thumb/c/c3/Hexammine_nickel_chloride%2C_bulk.jpg/270px-Hexammine_nickel_chloride%2C_bulk.jpg)

