Dégradation de Wohl
La dégradation de Wohl est une réaction de réduction de la longueur de la chaîne carbonée des aldoses[1], dont l'exemple le plus classique est la conversion du glucose en arabinose présentée ci-dessous. Cette réaction est nommée d'après le chimiste allemand Alfred Wohl.
Mécanisme
modifier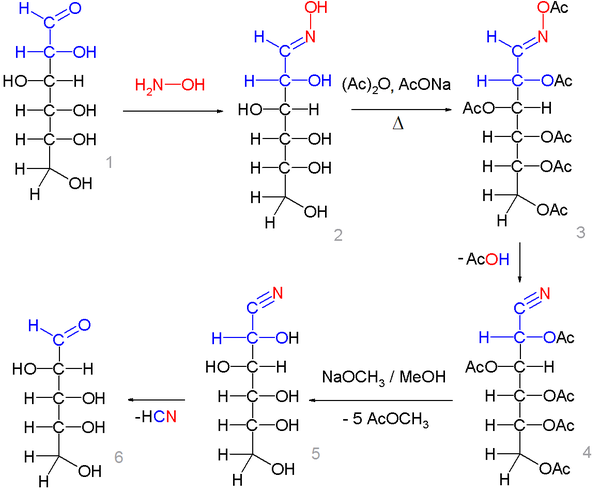
Dans la première étape[2],[3], le D-glucose (1) est converti en oxime de glucose (2) par réaction avec l'hydroxylamine et le méthanolate de sodium. Dans une deuxième étape, l'oxyme est mis à réagir avec l'anhydride acétique dans l'acétate de sodium avec chauffage. Cela produit une acétylation de tous les groupes alcools (estérification) ainsi que du groupe oxyme (3), produisant un composé instable ; finalement, l'acétate d'oxime se convertit en un nitrile, le glycononitrile de pentaacétyle (4).
Dans la dernière étape, le composé est mis à réagir avec le méthanolate de sodium dans le méthanol, provoquant la saponification de tous les groupes acétate (5) ainsi que le départ du groupe nitrile avec formation d'un groupe formyle.
Dégradation de Ruff-Fenton
modifierLa dégradation de Ruff-Fenton (Otto Ruff 1898, O. Fenton 1893) est une variation de la dégradation de Wohl qui convertit un aldose dans un premier temps en acide alpha-hydroxylé par réaction avec le dibrome et l'hydroxyde de calcium, puis cet acide est raccourci par réaction avec le sulfate de fer(III) et le peroxyde d'hydrogène[4].
Notes et références
modifier- (en) A. Wohl, Abbau des Traubenzuckers, 26, (DOI 10.1002/cber.189302601150), p. 730–744.
- Géza Braun, D-Arabinose, Org. Synth. 20, coll. « vol. 3 », , 14 p., p. 101.
- Pentaacetyl d-gluconitrile, Org. Synth. 20, coll. « vol. 3 », , 74 p., p. 690.
- Organic syntheses based on name reactions, Volume 22 Alfred Hassner,C. Stumer
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Wohl degradation » (voir la liste des auteurs).