Méthoxybenzaldéhyde
Le méthoxybenzaldéhyde, parfois aussi appelé anisaldéhyde est un composé organique aromatique de formule brute C8H8O2. Il est constitué d'une noyau de benzène substitué par un groupe méthoxyle (anisole) et un groupe formyle (benzaldéhyde). Comme tous les benzènes disubstitués, il existe sous la forme de trois isomères structuraux, les composés ortho, méta et para, selon la position relative des deux substituants sur le cycle :
- le 2-méthoxybenzaldéhyde, ou orthométhoxybenzaldéhyde ;
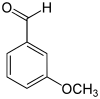
- le 3-méthoxybenzaldéhyde, ou métaméthoxybenzaldéhyde ;
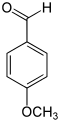
- le 4-méthoxybenzaldéhyde, paraméthoxybenzaldéhyde ou encore anisaldéhyde.
Nom
modifierOn rencontre parfois le terme « anisaldéhyde », notamment dans la littérature anglophone, comme synonyme de « méthoxybenzaldéhyde » (l'anisole étant le nom trivial du méthoxybenzène). Cependant, en règle générale et sans autre précision, le terme anisaldéhyde se réfère préférentiellement au dérivé para, le 4-méthoxybenzaldéhyde qui est le composé le plus courant dans l'industrie, que ce soit comme arôme, parfum, ou intermédiaire de synthèse dans l'industrie pharmaceutique.
Propriétés
modifier| Méthoxybenzaldéhyde | |||
| Nom | 2-méthoxybenzaldéhyde | 3-méthoxybenzaldéhyde | 4-méthoxybenzaldéhyde |
| Autre nom | orthométhoxybenzaldéhyde o-méthoxybenzaldéhyde |
métaméthoxybenzaldéhyde m-méthoxybenzaldéhyde |
paraméthoxybenzaldéhyde p-méthoxybenzaldéhyde anisaldéhyde |
| Représentation | 
|
|
|
| Numéro CAS | |||
| PubChem | 8658 | 11569 | 31244 |
| Formule brute | C8H8O2 | ||
| Masse molaire | 136,15 g·mol−1 | ||
| État | solide | liquide | |
| Apparence | solide jaunâtre à l'odeur caractéristique de réglisse |
liquide jaunâtre avec une odeur agréable |
liquide jaunâtre hautement volatil, sensible à la lumière et à l'air, à l'odeur caractéristique d'anis |
| Masse volumique | 1,127 g·cm-3[1] | 1,12 g·cm-3[2] | 1,12 g·cm-3[3] |
| Point de fusion | 34 à 40 °C[1] | 3 à 4 °C[4] | 0 à 2 °C[3] |
| Point d'ébullition | 238 °C[1] | 230 à 233 °C[2] | 248 °C[3] |
| Point d'éclair | 117 °C[1] | 110 °C[2] | 116 °C[3] |
| Point d'auto-inflammation | 225 °C[2] | 220 °C[3] | |
| Pression de vapeur saturante | 1,3 hPa (73 °C)[2] | <1 hPa (20 °C) 77 hPa (160 °C)[3] | |
| LogP | 1,71[2] | 1,65[3] | |
| Solubilité | Pratiquement insoluble dans l'eau, soluble dans l'éthanol et l'éther[1],[2],[3]. | ||
| SGH |
Pas de pictogramme SGH | ||
| Phrase H et P | Pas de phrase H ou P | ||
Occurrence naturelle
modifier
Le 2-méthoxybenzaldéhyde est naturellement présent dans le cannelier de Chine (Cinnamomum aromaticum)[5]. Le 3-méthoxybenzaldéhyde se trouve dans les fruits du giroflier[6]. Le 4-méthoxybenzaldéhyde peut être détecté dans le basilic[7], dans la menthe coréenne (Agastache rugosa)[8], le fenouil[8], la badiane[8] et l'anis[8].
Synthèse
modifierLes méthoxybenzaldéhydes peuvent être synthétisés par oxydation des méthoxytoluènes (méthylanisoles) correspondants, par exemple avec le dioxyde de manganèse qui va convertir le groupe méthyle en groupe aldéhyde. Le 4-méthoxybenzaldéhyde peut aussi être produit par clivage oxydant du groupe alcène de l'anéthol[9].
Utilisations
modifierLe 2-méthoxybenzaldéhyde est utilisé comme réactif pour synthétiser des bases de Schiff inhibitrices de la corrosion. Il est également utilisé comme arôme et ingrédient de parfum[10]. Structurellement proche de la vanilline, le 4-méthoxybenzaldéhyde est un produit largement utilisé dans l'industrie des parfums et des arômes[9]. Il est utilisé comme intermédiaire dans la synthèse d'autres composés importants pour les produits pharmaceutiques et la parfumerie.
Une solution de 4-méthoxybenzaldéhyde dans l'acide et l'éthanol est un colorant utile en chromatographie sur couche mince[11], différents composés sur la plaque pouvant donner différentes couleurs, ce qui permet de les distinguer facilement.
Dérivés
modifier- Hydroxyméthoxybenzaldéhyde (C8H8O3) : 10 isomères, dont la vanilline (4-hydroxy-3-méthoxybenzaldéhyde), l'isovanilline (3-hydroxy-4-méthoxybenzaldéhyde) et l'orthovanilline (2-hydroxy-3-méthoxybenzaldéhyde).
Notes et références
modifier- Entrée o-Anisaldehyde sur la base de données ChemBlink, consulté le 3 avril 2019.
- Entrée « 3-Methoxybenzaldehyde » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 3 avril 2019 (JavaScript nécessaire).
- Entrée « 4-Methoxybenzaldehyde » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 3 avril 2019 (JavaScript nécessaire).
- CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, (ISBN 0-8493-0303-6).
- Entrée O-ANISALDEHYDE, Dr. Duke's Phytochemical and Ethnobotanical Database, U.S. Department of Agriculture, lien
- Entrée 3-METHOXYBENZALDEHYDE, Dr. Duke's Phytochemical and Ethnobotanical Database, U.S. Department of Agriculture, lien
- Entrée P-METHOXYBENZALDEHYDE, Dr. Duke's Phytochemical and Ethnobotanical Database, U.S. Department of Agriculture, lien
- Entrée P-P-ANISALDEHYDE, Dr. Duke's Phytochemical and Ethnobotanical Database, U.S. Department of Agriculture, lien
- Ullmann's Encyclopedia of Industrial Chemistry, Weinheim, Wiley-VCH, (DOI 10.1002/14356007.a11_141), « Flavors and Fragrances »
- Collins I U et al., « Synthesis, experimental and computational studies on the anti-corrosion performance of substituted Schiff bases of 2-methoxybenzaldehyde for mild steel in HCl medium », Scientific Reports, vol. 13, , p. 3265 (DOI 10.1038/s41598-023-30396-3)
- Stains for Developing TLC Plates