Péplomère
Un péplomère ou spicule[2],[3], protéine S, protéine de pointe ou, par anglicisme, protéine spike, est une glycoprotéine prenant la forme d'un champignon émergeant de l'enveloppe virale (capside) de certains virus[4].


La protéine est glycosylée (ses glycanes étant ici représenté en orange)[1].
Ces protubérances ne se lient qu'à certains récepteurs de la cellule hôte ; elles sont essentielles à la fois pour la spécificité de l'hôte et l'infectiosité virale.
Dans le cas du coronavirus responsable de la COVID-19, le SARS-CoV-2, grâce à une triple articulation, ces "pointes" sont mobiles, ce qui ne semble pas être le cas des péplomères de virus grippaux, mais qui pourrait être le cas de tous les coronavirus (ce qui reste à démontrer).
Ces articulations confèrent une flexibilité aux protéines Spike qui peuvent ainsi « basculer, se balancer et tourner, ce qui pourrait leur permettre de scanner plus facilement la surface cellulaire et de permettre à plusieurs pointes de se lier à une même cellule humaine via des protéines ACE2 (réceptrices du virus) proches[5]. Il n'y a pas de données expérimentales similaires pour d'autres coronavirus, mais comme les séquences de protéines de pointe sont hautement conservées au cours de l'évolution, il est juste de supposer que ce trait est partagé »[6], précise Martin Beck du Max Planck Institute de biophysique de Frankfort qui a étudié ce sujet avec ses collègues[7].
Étymologie, terminologie
modifier(du grec πέπλος peplos, la tunique, ayant donné le terme péplos, désignant l'enveloppe des virus.)
Le mot « péplomère » désigne un groupement de protéines hétérologues[8] émergeant de la surface du virus et qui fonctionnent ensemble[réf. nécessaire].
Importance pour le système immunitaire
modifierLes « protéines S » sont la cible principale de la réponse immunitaire cellulaire et humorale ; elles induisent la formation d'anticorps.
Défenses contre le système immunitaire
modifierComme la majorité des protéines de surface, le péplomère a des régions hypervariables lui permettant de contourner les mécanismes de défense du système immunitaire[9].
D'autre part, le péplomère peut être, hormis pour sa zone active située à l'extrémité de la « pointe » (forme de « massue » en réalité), couvert de glycanes[6]. De nombreux virus ont des glycanes recouvrant leurs protéines externes, ce manteau constitué de sucres offre au virus, au moins dans un premier temps, une quasi-invisibilité face au système immunitaire humain (« comme un loup déguisé en mouton » note Megan Scudellari dans la Revue Nature)[6].
Chez les bactériophages
modifierLes fibres caudales de certains bactériophages, en particulier les phages de type T4, sont des péplomères modifiés.
Exemples
modifierLes péplomères peuvent être observés par microscopie électronique à la surface des virus enveloppés tels les Orthomyxoviridae, Paramyxoviridae, Rhabdoviridae, Filoviridae, Coronaviridae, Bunyavirodae, Arenaviridae et Retroviridae[10].
Cas particulier des virus grippaux
modifierLe virus de la grippe présente deux types de péplomères :
- l'hémagglutinine, triangulaire en forme de pointe ;
- la neuraminidase en forme de champignon[réf. nécessaire].
Cas particulier du SARS-CoV-2
modifier
Les progrès de la chimie, de la biophysique et de la biochimie computationnelles ont permis à Janet Iwasa (Université publique de l’Utah à Salt Lake City) et à son équipe de modéliser finement les parties externes du virus SARS-CoV-2 responsable de la pandémie de COVID-19 en se basant sur les données structurelles et génétiques disponibles en 2020[6]. Ces données ont permis à un superordinateur de produire un rendu « atome par atome » montrant bien que les protéines de pointe du SRAS-CoV-2 qui sortent de la capside sont non-rigides et qu’elles sont enveloppées d’un manteau constitué de petites molécules de sucre, dites glycanes[6].
Le virus de la COVID-19 a des protéines de pointes qui semblent inhabituellement mobiles (grâce à 3 articulations), alors que celle du virus de la grippe (autre gros virus aéroporté à ARN) sont rigides[6].
Cette modélisation a aussi permis de comprendre comment le virus, via un système bio-nano-mécanique, peut s’arrimer aussi solidement sur les cellules humaines qu’il cible « avec une force surprenante » (par rapport au SARS-CoV-1, le SARS-CoV-2 se lie à l'ACE2 environ 2 à 4 fois plus solidement)[11], puis à se cacher dans la cellule, puis à se déguiser quand les virions en repartent, expliquant son infectiosité et la difficulté que le système immunitaire a à le contrôler[6].
Les mutations de cette protéine sont suivies avec attention par les virologues et les fabricants de vaccins. À titre d'exemple :
- le variant Alpha du SARS-CoV-2 présente dix changements de configuration de la protéine Spike, faisant que le RBD (Receptor binding domain, domaine d'une protéine lui permettant de se lier au récepteur ciblé) tend à se présenter plus souvent en position « haute »[12] ; ce qui aiderait le virus à pénétrer ses cellules cibles, selon Priyamvada Acharya (biologiste structurale au Duke Human Vaccine Institute de Durham, en Caroline du Nord) ;
- le variant Delta est quant à lui porteur de plusieurs mutations de la sous-unité S1, dont 3 dans le RBD qui semblent faciliter sa capacité à se lier à l'ACE2 et à échapper au système immunitaire[13].
Galerie d'images
modifier-
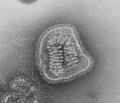
Protéines Spike visibles en microscopie électronique.
-
Particule virale de la grippe (Influenza).
-
VIH (virus du SIDA).
Notes et références
modifier- (ru) Alexey Solodovnikov et Valeria Arkhipova, « Достоверно красиво: как мы сделали 3D-модель SARS-CoV-2 » [« Truly beautiful: how we made the SARS-CoV-2 3D model »] [archive du ], N+1, (consulté le )
- « Chapitre 1 - Structure des virus, cycle viral, physiopathologie des infections virales », sur Médecine Sorbonne Université (consulté le ).
- « Initiation à la virologie. Structure de la particule virale », sur Université catholique de Louvain (consulté le ).
- (en) Saunders Comprehensive Veterinary Dictionary, Elsevier, Inc, (lire en ligne)
- (en) Beata Turoňová et Mateusz Sikora, « In situ structural analysis of SARS-CoV-2 spike reveals flexibility mediated by three hinges », sur Science (New York, N.y.), (PMID 32817270, DOI 10.1126/science.abd5223, consulté le ), p. 203
- (en) Megan Scudellari, « How the coronavirus infects cells — and why Delta is so dangerous », Nature, vol. 595, no 7869, , p. 640–644 (ISSN 0028-0836 et 1476-4687, DOI 10.1038/d41586-021-02039-y, lire en ligne, consulté le )
- (en) Beata Turoňová, Mateusz Sikora, Christoph Schürmann et Wim J. H. Hagen, « In situ structural analysis of SARS-CoV-2 spike reveals flexibility mediated by three hinges », Science, vol. 370, no 6513, , p. 203–208 (ISSN 0036-8075 et 1095-9203, PMID 32817270, PMCID PMC7665311, DOI 10.1126/science.abd5223, lire en ligne, consulté le )
- Relatif aux tissus, aux sérums et aux cellules qui proviennent d'un individu d'une espèce différente.
- (en) « Changement de tropisme des coronavirus », Revue Francophone des Laboratoires, vol. 2010, no 423, , p. 63–68 (ISSN 1773-035X, DOI 10.1016/S1773-035X(10)70561-X, lire en ligne, consulté le )
- (en) Christopher J. Burrell, Colin R. Howard, Frederick A. Murphy, Fenner and White’s Medical Virology, CInquième édition,
- Hoang Linh Nguyen et Pham Dang Lan, « Does SARS-CoV-2 Bind to Human ACE2 More Strongly Than Does SARS-CoV? », sur The Journal of Physical Chemistry B, (ISSN 1520-6106, DOI 10.1021/acs.jpcb.0c04511, consulté le ), p. 7336–7347
- (en) Sophie M.-C. Gobeil et Katarzyna Janowska, « Effect of natural mutations of SARS-CoV-2 on spike structure, conformation, and antigenicity », sur Science, (ISSN 0036-8075, PMID 34168071, PMCID PMC8611377, DOI 10.1126/science.abi6226, consulté le ), eabi6226
- Jasmin Khateeb, Yuchong Li et Haibo Zhang, « Emerging SARS-CoV-2 variants of concern and potential intervention approaches », Critical Care, vol. 25, no 1, (ISSN 1364-8535, DOI 10.1186/s13054-021-03662-x, lire en ligne, consulté le )
Voir aussi
modifierArticles connexes
modifier- Glycoprotéine
- Récepteur (biochimie)
- Phage T4
- Entrée virale
- Cycle de vie viral