tert-Butoxycarbonyle
Le groupe fonctionnel tert-butoxycarbonyle, beaucoup plus connu sous son acronyme BOC ou Boc, est un groupe protecteur des amines. Sa formule moléculaire est (CH3)3C–O–C(=O)– et il forme un carbamate en s'ajoutant sur une amine. Il est utilisé en particulier comme groupement protecteur de fonctions amines (α-amine ou chaîne latérale, le cas échéant) des acides aminés dans la synthèse peptidique.
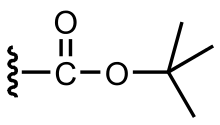
Le groupe BOC ne réagit pas avec la plupart des bases et des nucléophiles, permettant une protection orthogonale avec Fmoc.
Protection et déprotection
modifierLe groupe BOC peut être ajouté sur les amines en solution aqueuse en utilisant le dicarbonate de di-tert-butyle (BOC2O) en présence d'une base comme le bicarbonate de sodium (NaHCO3). La protection des amines peut aussi être effectuée dans l'acétonitrile en utilisant de la 4-diméthylaminopyridine (DMAP) comme base. Le chloroformiate de tert-butyle, BOCCl, est un autre composé qui permet l'introduction de BOC.
L'élimination de BOC sur les acides aminés peut être accompli avec les acides forts comme l'acide trifluoroacétique pur ou dans le dichlorométhane, ou comme du chlorure d'hydrogène (HCl) dans le méthanol[1],[2],[3]. Il peut aussi être retiré en utilisant K2CO3 dans le méthanol à température ambiante[4].
Autre usage
modifierLa synthèse à partir de la 2-pipéridone (1) de la 6-acétyl-2,3,4,5-tétrahydropyridine (5 ci-dessous), un composé important de l'arôme de pain, a été accomplie en utilisant le groupe BOC introduit par l'anhydride de BOC (BOC2O), dans une réaction de Maillard[5]. La première étape de cette synthèse est la formation du carbamate (2), par réaction entre l'amine secondaire et l'anhydride de BOC dans l'acétonitrile avec la DMAP comme base.
Notes et références
modifier- Robert M. Williams, Peter J. Sinclair, Duane E. DeMong, Daimo Chen, and Dongguan Zhai, 4-Morpholinecarboxylic acid, 6-oxo-2,3-diphenyl-, 1,1-dimethylethyl ester, (2S,3R)-, Org. Synth. 80, coll. « vol. », , 18 p.
- (en) E. A. Englund, H. N. Gopi, D. H. Appella, « An Efficient Synthesis of a Probe for Protein Function: 2,3-Diaminopropionic Acid with Orthogonal Protecting Groups », Org. Lett., vol. 6, no 2, , p. 213–215 (PMID 14723531, DOI 10.1021/ol0361599)
- (en) D. M. Shendage, R. Fröhlich, G. Haufe, « Highly Efficient Stereoconservative Amidation and Deamidation of α-Amino Acids », Org. Lett., vol. 6, no 21, , p. 3675–3678 (PMID 15469321, DOI 10.1021/ol048771l)
- (en) Saul Jaime-Figueroa, Alejandro Zamilpa, Angel Guzma´n,and David J. Morgans,Jr., « N-3-Alkylation of uracil and derivatives via N-1-BOC protection », Synthetic Communications, vol. 31, no 24, , p. 3739–3746 (DOI 10.1081/SCC-100108223)
- (en) Tyler J. Harrison and Gregory R. Dake, « An Expeditious, High-Yielding Construction of the Food Aroma Compounds 6-Acetyl-1,2,3,4-tetrahydropyridine and 2-Acetyl-1-pyrroline », J. Org. Chem., vol. 70, no 26, , p. 10872–10874 (PMID 16356012, DOI 10.1021/jo051940a)
Voir aussi
modifierArticles connexes
modifierLiens externes
modifier- Conditions de protection et déprotection - protocoles de synthèse sur organic-reaction.com

