Virus de la grippe A
Alphainfluenzavirus influenzae
| Domaine | Riboviria |
|---|---|
| Embranchement | Negarnaviricota |
| Sous-embr. | Polyploviricotina |
| Classe | Insthoviricetes |
| Ordre | Articulavirales |
| Famille | Orthomyxoviridae |
| Genre | Alphainfluenzavirus |
- Espèce : virus de la grippe A
- sous-type H1N1
- sous-type H1N2
- sous-type H2N2
- sous-type H2N3
- sous-type H3N1
- sous-type H3N2
- sous-type H3N8
- sous-type H5N1
- sous-type H5N2
- sous-type H5N3
- sous-type H5N6
- sous-type H5N8
- sous-type H5N9
- sous-type H6N1
- sous-type H6N2
- sous-type H7N1
- sous-type H7N2
- sous-type H7N3
- sous-type H7N4
- sous-type H7N7
- sous-type H7N9
- sous-type H9N2
- sous-type H10N7
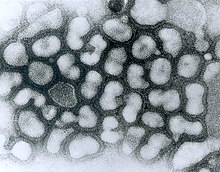
micrographie à transmission électronique de
particules virales chargées négativement en
passage tardif. (Source : Dr Erskine Palmer,
bibliothèque d’images du Centers for Disease
Control and Prevention Public Health,
image no 280). Date de création : 1981.
Le virus de la grippe A, dont le nom scientifique depuis 2021 est Alphainfluenzavirus influenzae (anciennement Influenza A virus), est un virus à ARN monocaténaire de polarité négative à génome segmenté (8 segments) qui appartient au genre Alphainfluenzavirus de la famille des Orthomyxoviridae. Il présente un grand nombre de sous-types identifiés par deux antigènes présents à sa surface, l'hémagglutinine et la neuraminidase, selon une notation indiquant les types d'antigènes du virus : par exemple, le sous-type H5N1 fait référence à la présence d'hémagglutinine de type 5 et de neuraminidase de type 1. On connaît 18 antigènes H, notés de H1 à H18, et 11 antigènes N, notés de N1 à N11[2],[3]. Le sous-type H17N10 a été observé chez des roussettes en 2012[4], tandis que le sous-type H18N11 a été observé chez une chauve-souris du Pérou en 2013[3].
Tous ces sous-types ont été isolés chez des oiseaux sauvages, chez lesquels il est susceptible de provoquer la grippe aviaire, bien que cette maladie soit en réalité assez rare. Certains de ces virus peuvent être très pathogènes et provoquer une maladie grave chez les volailles et, plus rarement, chez l'homme[5]. Il peut arriver que le virus soit transmis aux volailles par des oiseaux sauvages et, de là, contamine des humains, provoquant des épidémies, voire des pandémies[6],[7].
Comme tous les virus à ARN, les virus de la grippe A tendent à muter, de sorte que chaque sous-type s'est diversifié en souches plus ou moins pathogènes, dont la pathogénicité varie fortement d'une espèce animale à une autre.
Sous-types et variantes
modifier
Les virus de la grippe A sont des virus à ARN classés en sous-types en fonction du type de deux protéines de leur enveloppe virale :
- l'hémagglutinine, notée H, nommée ainsi car elle provoque l'agglutination des globules rouges ;
- la neuraminidase, notée N, enzyme clivant les liaisons osidiques des acides sialiques, dont le principal est l'acide N-acétylneuraminique.
L'hémagglutinine joue un rôle central dans la reconnaissance et la liaison du virus aux cellules hôtes, ainsi que dans l'infection de la cellule par son ARN. La neuraminidase, en revanche, est essentielle à la libération subséquente des particules virales produites au sein de la cellule infectée pour contaminer d'autres cellules.
Différents virus de la grippe codent différentes protéines d'hémagglutinine et de neuraminidase. Ainsi, le sous-type H5N1 désigne un sous-type de virus de la grippe A dont l'enveloppe contient de l'hémagglutinine (H) de type 5 et de la neuraminidase (N) de type 1. Il existe 18 types d'hémagglutinine et 11 types de neuraminidase, de sorte qu'il existe théoriquement 198 combinaisons différentes de ces protéines[2],[3].
Certaines variantes peuvent être nommées en fonction de l'isolat dont elles peuvent être rapprochées et dont on présume qu'elles partagent la même lignée, comme les virus de type grippe de Fujian, en fonction de leur hôte, comme le virus de la grippe humaine, en fonction de leur sous-type, comme le virus H3N2, ou en fonction de leur pathogénicité, par exemple l'indication LP signifiant low pathogenicity (« faible pathogénicité »). Ainsi, une grippe provoquée par un virus semblable à l'isolat A/Fujian/411/2002(H3N2) peut être qualifiée aussi bien de grippe Fujian, de grippe humaine et de grippe H3N2.
Des variantes du virus de la grippe peuvent également être nommées en fonction de l'hôte chez lequel la souche est endémique ou auquel elle est adaptée. Ce sont notamment :
- la grippe aviaire, endémique chez des oiseaux ;
- la grippe canine, endémique chez des chiens ;
- la grippe équine, endémique chez des chevaux ;
- la grippe porcine, endémique chez des porcs.
Les grippes aviaires sont parfois distinguées en fonction de leur pathogénicité pour les volailles, notamment chez les poulets :
- LPAI : low pathogenic avian influenza, « grippe aviaire faiblement pathogène » ;
- HPAI : highly pathogenic avian influenza, « grippe aviaire hautement pathogène ».
Compte tenu de la rapidité de mutation des virus de la grippe, la plupart des souches répertoriées sont à présent éteintes. Par exemple, le sous-type H3N2 de grippe saisonnière ne contient plus la souche à l'origine de la grippe de Hong Kong.
Sous-types
modifierH1N1
modifierLes virus de la grippe A (H1N1) sont régulièrement responsables des cas de grippe saisonnière. Certaines souches de H1N1 sont endémiques aux humains, tandis que d'autres sont endémiques chez les oiseaux (grippe aviaire) et chez les porcs (la grippe porcine).
Des virus du sous-type H1N1 sont responsables des pandémies de grippe en 1918 et en 2009. Les symptômes sont similaires à ceux de la grippe saisonnière et peuvent inclure fièvre, éternuements, mal de gorge, toux, maux de tête et douleurs musculaires et articulaires.
H1N2
modifierH1N8
modifierH2N2
modifierLe sous-type H2N2 serait responsable de l'épidémie de grippe en 1889 en Russie.
Des virus H2N2 ont muté en différentes souches, incluant la souche de la grippe asiatique entre 1956 et 1958, les H3N2, et d'autres souches se retrouvant dans les oiseaux.
H2N3
modifierH3N1
modifierH3N2
modifierLa grippe de 1968 a été causée par un virus de sous-type H2N2 réassorti en sous-type H3N2.
H3N3
modifierH3N8
modifierH4N1
modifierH5N1
modifierLe sous-type H5N1 peut être hautement pathogène et responsable d'épizooties de grippe aviaire. La première apparition connue de ce type de grippe chez les humains a eu lieu à Hong Kong en 1997. L’infection des humains a coïncidé avec une épizootie de grippe aviaire, causée par le même agent infectieux, dans les élevages de poulets à Hong Kong.
Des variantes faiblement pathogènes du H5N1 ont également été repérées.
H5N2
modifierH5N3
modifierH5N6
modifierCe sous-type a été signalé en chez des volailles en Chine mais a aussi été détecté en Asie du Sud-Est (Laos et Vietnam).
La première victime humaine signalée l'a été en Chine début 2014[8]. En , la FAO la considère comme une nouvelle menace pour la santé animale[9]. Son statut en termes de risques écoépidémiolgiques est en discussion. Il serait au moins pour certains variants hautement pathogène selon l’OIE (exemple : 498 faisans de Colchide morts et 60 abattus sur un total de 558 faisans en aout 2014 au Vietnam)[10].
H5N8
modifierLe sous-type H5N8, autrefois considéré comme l'un des sous-types peu pathogènes et à faible risque de le devenir, est surveillé car plusieurs fois il a joué un rôle d’incubateur naturel pour le virus H1N1 hautement pathogène[11].
H5N9
modifierUn variant hautement pathogène du sous-type H5N9 a déjà dérivé d'un virus faiblement pathogène du sous-type H5N1 dans certains élevages (A/turkey/Ontario/6213/1966 ; H5N1)[12].
H6N1
modifierH6N2
modifierH7
modifierLe sous-type H7 affecte principalement les oiseaux mais des cas humains ont été repérés au Canada en 2004[13].
H7N1
modifierH7N2
modifierH7N3
modifierH7N4
modifierH7N7
modifierH7N9
modifierReconnu en Chine le , selon les autorités officielles.
H9N2
modifierH10N7
modifierLe sous-type H10N7 est signalé pour la première fois chez l'homme en 2004, en Égypte[14]. Deux enfants d'un an tombent malades. Les deux résident à Ismaïlia, en Égypte, et le père de l'un d'eux est vendeur de volailles[15].
La première épizootie aux États-Unis d'Amérique survient dans deux élevages de dindes au Minnesota, en 1979. Un troisième élevage est affecté en 1980. Le spectre des symptômes va du très grave, avec un taux de mortalité atteignant 31 %, jusqu'au subclinique. Des virus au profil antigénique indistinguable de ceux des dindes infectées ont été isolés sur des canards colverts présents dans une mare adjacente à l'élevage des dindes[16].
Le sous-type H10N7 semble avoir été impliqué dans une mortalité massive de phoques en Europe du nord en 2014[17],[18].
H10N8
modifierLe sous-type H10N8 est encore mal connu. Le , la Chine a confirmé qu'une patiente de 75 ans (morte d'une pneumonie sévère dans la province du Jiangxi) était le 1er cas connu d'infection humaine H10N8[19] ; deux mois plus tard dans la même province du Jiangxi (le ) trois autres cas humains de H10N8 étaient ont été confirmés (dont deux mortels)[19].
Un article de la revue Clinical Infectious Diseases a signalé que dans la province du Guangdong (Chine) des chiens errants dans des marchés de volaille ont pour la première fois montré des signes tangibles d'infections par le sous-type viral H10N8 alors qu'au même moment une épizootie due au H5N8 s'étend en Asie, laissant penser que l'organisme du chien pourrait être un lieu de réassortiment génétique pour plusieurs souches virales en circulation[19].
H11N2
modifierH11N9
modifierH17N10
modifierH18N11
modifierVoir aussi
modifierArticles connexes
modifier- Grippe (alias influenza ou flu en anglais)
- Grippe aviaire (alias peste aviaire) : épidémiologie - Historique - Souches animales - Prévalence - Risque pandémique lié à la grippe aviaire - Histoire des épizooties de grippe aviaire - Pandémie grippale - Grippe espagnole.
- Virus de la grippe B
- Virus de la grippe C
- Virus de la grippe D
- Grippe féline
- Grippe canine
- Grippe équine
- Épizootie
- Zoonose
- Épidémiologie, écoépidémiologie
- Liste von Subtypen des Influenza-A-Virus (de)
- Cheval de Troie (virus)
Notes et références
modifier- (en) « Virus Taxonomy: 2023 Release », ICTV, (consulté le ).
- (en) « Influenza Type A Viruses », CDC, (consulté le ).
- (en) Suxiang Tong, Xueyong Zhu, Yan Li, Mang Shi, Jing Zhang, Melissa Bourgeois, Hua Yang, Xianfeng Chen, Sergio Recuenco, Jorge Gomez, Li-Mei Chen, Adam Johnson, Ying Tao, Cyrille Dreyfus, Wenli Yu, Ryan McBride, Paul J. Carney, Amy T. Gilbert, Jessie Chang, Zhu Guo, Charles T. Davis, James C. Paulson, James Stevens, Charles E. Rupprecht, Edward C. Holmes, Ian A. Wilson, Ruben O. Donis, « New World Bats Harbor Diverse Influenza A Viruses », PLoS Pathogens, vol. 9, no 10, , article no e1003657 (PMID 24130481, PMCID 3794996, DOI 10.1371/journal.ppat.1003657, lire en ligne).
- (en) Suxiang Tong, Yan Li, Pierre Rivailler, Christina Conrardy, Danilo A. Alvarez Castillo, Li-Mei Chen, Sergio Recuenco, James A. Ellison, Charles T. Davis, Ian A. York, Amy S. Turmelle, David Moran, Shannon Rogers, Mang Shi, Ying Tao, Michael R. Weil, Kevin Tang, Lori A. Rowe, Scott Sammons, Xiyan Xu, Michael Frace, Kim A. Lindblade, Nancy J. Cox, Larry J. Anderson, Charles E. Rupprecht et Ruben O. Donis, « A distinct lineage of influenza A virus from bats », Proceedings of the National Academy of Sciences of the United States of America, vol. 109, no 11, , p. 4269-4274 (PMID 22371588, PMCID 3306675, DOI 10.1073/pnas.1116200109, Bibcode 2012PNAS..109.4269T, lire en ligne).
- « Grippe aviaire et autres grippes zoonotiques », OMS, (consulté le ).
- (en) H. Klenk, M. Matrosovich et J. Stech, « Avian Influenza: Molecular Mechanisms of Pathogenesis and Host Range », Animal Viruses: Molecular Biology, dirigé par T. C. Mettenleiter et F. Sobrino, Caister Academic Press, 2008. (ISBN 978-1-904455-22-6).
- (en) Y. Kawaoka, Influenza Virology: Current Topics, Caister Academic Press, 2006. (ISBN 978-1-904455-06-6).
- Chinela gripe aviaire H5N6 fait une première victime, 7 mai 2014.
- Rome – Une souche du virus de la grippe apparue récemment chez la volaille en Asie du Sud-Est et baptisée A(H5N6) constitue une nouvelle menace pour la santé animale et les moyens d'existence qui doit être surveillée de près, a mis en garde la FAO aujourd'hui 22 septembre 2014.
- Un foyer de grippe aviaire A/H5N6 à Lao Cai; vietnamplus, 2014-08-23.
- "RCI Inactivation of Avian Influenza". http://www.activtek.eu.
- Jihui Ping & al. (2012), « Low-pathogenic avian influenza virus A/turkey/Ontario/6213/1966 (H5N1) is the progenitor of highly pathogenic A/turkey/Ontario/7732/1966 (H5N9) ». • J. Gen. Virol., August 2012 93: 1649-1657, doi: 10.1099/vir.0.042895-0, Online: 01/08/2012 (résumé).
- Cas humains de grippe A(H7) sur le site de l'OMS.
- (en) P. F. Wright, G. Neumann et Y. Kawaoka, Fields Virology, vol. 1, Philadelphia, PA, Wolters Kluwer/Lippincott Williams & Wilkins, , 6e éd., 1201 p. (ISBN 978-1-4511-0563-6), « 41-Orthomyxoviruses ».
- (en) « EID Weekly Updates - Emerging and Reemerging Infectious Diseases, Region of the Americas », Pan American Health Organization, (consulté le ).
- (en) D. Karunakaran, V. Hinshaw, P. Poss, J. Newman et D. Halvorson, « Influenza A outbreaks in Minnesota turkeys due to subtype H10N7 and possible transmission by waterfowl », American Association of Avian Pathologists, Inc., vol. 27, no 2, , p. 357–66 (PMID 6870718, DOI 10.2307/1590162, JSTOR 1590162).
- (en) S Zohari, A Neimanis, T Härkönen et C Moraeus, « Avian influenza A(H10N7) virus involvement in mass mortality of harbour seals (Phoca vitulina) in Sweden, March through October 2014 », Eurosurveillance, vol. 19, no 46, (ISSN 1560-7917, DOI 10.2807/1560-7917.ES2014.19.46.20967, lire en ligne, consulté le ).
- Rogier Bodewes, Theo M. Bestebroer, Erhard van der Vries et Josanne H. Verhagen, « Avian Influenza A(H10N7) Virus–Associated Mass Deaths among Harbor Seals », Emerging Infectious Diseases, vol. 21, no 4, , p. 720–722 (ISSN 1080-6040 et 1080-6059, PMID 25811303, PMCID PMC4378483, DOI 10.3201/eid2104.141675, lire en ligne, consulté le ).
- (en) Shuo Su et al. « First Evidence of H10N8 Avian Influenza Virus Infections among Feral Dogs in Live Poultry Markets in Guangdong Province, China » Clin Infect Dis. 2014;59(5):748-50. DOI 10.1093/cid/ciu345.
