Gaz manufacturé
Les gaz manufacturés désignent des gaz qui ont été fabriqués à partir de 1880, date de leur invention, dans des usines à gaz. Ils sont utilisés d'abord comme gaz d'éclairage, par la suite comme combustible pour les turbines et moteurs, pour le chauffage ainsi que la cuisson. Ces gaz furent remplacés par l'électricité dans leurs applications d'éclairage à partir de 1880, dans les autres applications par le gaz naturel aux environs de 1960. L'histoire du gaz manufacturé est liée à l'histoire de nos villes et des grands groupe énergétiques modernes.
Histoire
L'émergence du gaz d'éclairage et des gaz manufacturé est le résultat des recherches et inventions conjuguées du français Philippe Lebon, de l'anglais William Murdoch et de l'allemand Frédéric-Albert Winsor.
Définitions
Distillation
La plupart des gaz manufacturés historique sont obtenus par distillation, c'est le terme qui est très largement utilisé dans les traités scientifiques du XIXe siècle. Il s'agirait en fait plutôt d' une pyrolyse (ou craquage thermique ou Cokéfaction Distillation sèche, en anglais: Distillation destructive). Dans l'acceptation moderne, la pyrolyse est la décomposition d'un composé organique par la chaleur pour obtenir d'autres produits (gaz et matière) qu'il ne contenait pas. La distillation est lui un procédé de séparation constituants d'un mélange homogène dont les températures d'ébullition sont différentes)
Usine à gaz et cokeries
Les usine à gaz sont les usines qui furent mises en œuvre pour la production des gaz manufacturés, généralement à partir de houille (gaz de houille). Dans les usines à gaz, le coke, combustible précieux pour la sidérurgie est un sous produit de la production du gaz de houille.
Dans les cokeries, qui deviendront le principal fournisseur de gaz de ville par la suite, le gaz de houille, est un sous produit de la production du coke à partir de la houille.
Le coke est principalement utilisé en sidérurgie.
Les usines à gaz sont abandonnées à partir de 1930.
Gazomètre
Un gazomètre est un réservoir servant à stocker le gaz manufacturé ou le gaz naturel à température ambiante et à une pression proche de la pression atmosphérique. Le volume du réservoir varie selon la quantité de gaz qu'il contient, la pression étant assurée par une cloche mobile verticalement. Les plus grands gazomètres ont des capacités allant jusqu'à 350 000 m³, pour des structures atteignant plus de 60 mètres de diamètre.
Gaz d'éclairage
Les premiers gaz manufacturés servent à l'éclairage des villes et prennent donc le nom de gaz d'éclairage
Gaz de ville
Le gaz d'éclairage sert par la suite de combustible pour les turbines et moteurs, pour le chauffage ainsi que la cuisson. L'appellation gaz de ville, provient du fait que le gaz d'éclairage est essentiellement distribué dans les villes et ne sert désormais plus seulement à s'éclairer.. De nos jours l'appellation gaz de ville recouvre indifféremment et selon les régions, le gaz produit à partir de la houille, ou le gaz naturel distribué à l'usager[1].
Gaz de bois
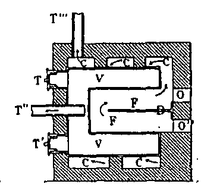
C'est le gaz mis au point entre 1785 et 1786, par l'ingénieur Philippe Lebon, en France obtenu par distillation du bois.
En chauffant le bois Lebon obtient un gaz malodorant qu'il appelle gaz hydrogène ou gaz hydrogène carburé, nom qui va lui rester pendant près de trente ans.
La majorité des composants du bois sec ne sont pas distillables : En effet, le bois est constitué principalement de macromolécules: Cellulose (environ 50 %), Lignine (20 à 30 %), Hémicellulose (15 à 25 %). Pour le reste différentes matières organiques : polysaccharides, pentosanes, hexosanes, résines, tannins, colorants, cires, alcaloïdes, ainsi que d'un faible pourcentage (de 1 à 1,5 %) d'éléments minéraux)[2]. Pour les résineux, on observe une faible quantité de résines, de l’ordre de 3%, qui seules peuvent donner lieu à un vrai distillat.
La Composition chimique du bois (50 % de carbone, 42 % d'oxygène, 6 % d'hydrogène, 1 % d'azote et 1 % de cendre) montre que, contrairement à la houille, dans le bois même parfaitement sec, l’oxygène représente plus du tiers du poids total, ce qui est un handicap certain[3]..
La distillation (pyrolyse) du bois permet généralement d'obtenir les produits suivants[4][3]:
- un gaz lavé, combustible et éclairant, constitué d'hydrogène(H2), monoxyde de carbone(CO), Dioxyde de carbone (CO2). A noter que le monoxyde de carbone(CO), bien que très toxique, participe activement à la combustion en ne donnant que du gaz carbonique (CO2). La présence de CO2 par contre tend à diminuer sensiblement le pouvoir éclairant du gaz.
- Des vapeurs condensables: eau, méthanol (longtemps appelé alcool de bois), des acides acétiques et acide formiques, du phénol, des aldéhydes légers,; Les liquides obtenus par condensation de ces gaz se séparent par décantation en une couche aqueuse supérieure, le jus pyroligneux(d’une odeur acre insoutenable, formé de l’ensemble des produits volatils) et une couche inférieure, les goudrons. Le goudron constitue un précieux matériau pour le calfatage des navires lorsqu’il provient de résineux.
- Un solide, assimilable au charbon de bois(teneur en carbone de l'ordre de 80%)
Lebon ne se borne pas à découvrir le gaz, il le met en pratique. Sa Thermolampe trouve sa première application avec l'éclairage de la ville de Paris. Il installe pour la première fois ce système dans l'hôtel de Seigneley à Paris le 11 octobre 1801[5]. Le système se compose d'un vaste four à bois dont les gaz produits par distillation sont acheminés dans les différentes pièces de l'hôtel par différents tuyaux pour les éclairer, tandis que l'hôtel est chauffé par la chaleur produite par le four.
Son système et la mauvaise qualité de son gaz ne connaissent pas le succès escompté.
Gaz de houille
Philippe Lebon, mort prématurément, sera lu par ses successeurs anglais et allemand, William Murdoch et Frédéric-Albert Winsor, qui seront à l'origine de l'essor de l'industrie du gaz en Angleterre.
Ils fabriquent en Angleterre, un gaz à partir de la houille, le gaz de houille. Le Gaz de houille est nommé gaz light par William Murdoch, en France, "gaz hydrogène carburé". (Le gaz de houille ne doit pas être confondu avec le gaz de couche, un gaz, principalement constitué de méthane, qui est piégé (adsorbé) au cœur de la matrice solide du charbon dans les bassins houillers.)
La houille est loin de n’être que du carbone. Pour 10 atomes de carbone on y compte 8 atomes d’hydrogène en moyenne provenant d’hydrocarbures aromatiques condensés dérivés du naphtalène, de l’anthracène, du phénanthrène et de leurs homologues supérieurs. En outre elle renferme toujours plus ou moins de soufre qui conduit, lors de la cokéfaction, à un gaz particulièrement toxique et malodorant, le sulfure d'hydrogène H2S[3].
La distillation (pyrolyse) du charbon permet d'obtenir[6],[3]:
- Un gaz brut riche en hydrogène(H2), méthane(CH4), monoxyde de carbone(CO) ; un peu de Dioxyde de carbone (CO2) ainsi que l’inévitable sulfure d'hydrogène (H2S) ; des traces de mercaptans et autres impuretés. Murdoch qui ignorait bien sûr le détail de cette composition appelait tout simplement son gaz le gas light (terme plus convenable que gaz hydrogène). Il en retirait environ 250 litres par kilogramme de charge.
- Un goudron de houille liquide riche en composés aromatiques et polyaromatiques alors utilisé pour le calfatage et qui deviendra le produit de base de la carbochimie (sa distillation à 400 °C permet d'obtenir du benzène, toluène, xylène, aniline, phénol, naphtalène et anthracène)
- 75% de carbone impur, le coke, restant dans la cornue, et dont la vente à elle seule couvrait le prix d’achat de la houille.
En 1807, Le gaz de houille avait des défauts multiples[3]:
- Une odeur pestilentielle due pour l’essentiel au sulfure d'hydrogène (H2S).
- le noircissement des peintures contenant de la céruse (carbonate basique de plomb) sous l’effet soit du H2S, soit de son produit de combustion le Dioxyde de soufre (SO2. De cet inconvénient naîtra toutefois un progrès : le développement (modeste) des peintures à base de blanc de zinc, beaucoup moins toxiques et ne noircissant pas.
- l’excès de Dioxyde de carbone(CO2) qui tend à diminuer le pouvoir éclairant.
- les résidus de goudron qui ont pour effet d’encrasser les canalisations.
- enfin la présence d’aérosols et d’une manière générale de condensables qui, avec les fluctuations de température, présentent la fâcheuse propriété de se rassembler, en phase liquide, dans les parties basses de l’installation, provoquant de graves perturbations dans le fonctionnement général du réseau. L’expression populaire "Y’a d’l’eau dans le gaz" nous en est restée pour signifier une situation assez conflictuelle.
Le gaz de houille devra subir des transformations d'épuration qui seront entièrement réalisées par l'anglais Samuel Clegg
Le gaz de houille obtenu dans une usine à gaz en 1970 a un pouvoir calorifique entre 5000 et 5800 calories/m3 (ce qui signifie qu'un m3 de gaz peut élever d'un degré la température de 5200 à 5800 litres d'eau). Le gaz est alors mélangé à une certaine quantité de gaz à l'air et de gaz à l'eau. Comme ces gaz ont un pouvoir calorifique plus faible, l'ensemble donne au gaz de ville un pouvoir calorifique plus faible entre 4000 et 5000 calories/m3. Le gaz épuré est incolore.
| En volume | En poids | |
|---|---|---|
| Hydrogène | 50% | 8,4% |
| Méthane | 32% | 41,6% |
| Oxyde de carbone | 8% | 18,8% |
| Éthylène et autres hydrocarbures | 4% | 9,4% |
| Azote | 3% | 7,1% |
| Anhydride carbonique | 2% | 7,4% |
| Benzol et produits voisins | 1% | 7,3% |
Gaz d'huile
La fabrication du gaz de l'huile a été découverte et établie en Angleterre par un certain Taylor.
« L'appareil que l'on emploie à cet effet est fort simple. Il se compose d'un cylindre de fonte que l'on porte au rouge naissant, et dans lequel on fait couler l'huile; le cylindre est rempli de pierres ou plus souvent de fragments de coke, afin de présenter plus de surface. Un tuyau fait arriver l'huile dans cet appareil; elle se réduit en vapeurs qui traversent toute la longueur du cylindre. A l'autre extrémité du cylindre se trouve adapté un second tuyau qui conduit le gaz dans un vase rempli d'huile, afin qu'il y dépose la portion huileuse qui a échappé à l'action de la chaleur; enfin de là il se rend dans un gazomètre d'où on le distribue suivant les besoins. Les produits de la décomposition des matières grasses par la méthode qui vient d'être décrite varient beaucoup suivant la température. Au rouge naissant, elles donnent, en ne laissant presque pas de résidu, de l'oxyde de carbone, du gaz oléfiant, des hydrogènes carbonés en vapeurs et fort volatils, du gaz des marais et de petites quantités d'hydrogène libre; à des températures plus élevées, on obtient plus de charbon; la quantité du gaz défiant et des autres hydrogènes carbonés diminue, celle du gaz des marais[7] »
augmente au contraire, de sorte que par là le pouvoir éclairant du produit s'affaiblit beaucoup.
Les expériences menées vers 1850 pour obtenir du gaz d'huile se sont avérées concluantes. « Des expériences de M. Faraday et de M. Thomas Dewis ont démontré que le pouvoir illuminant du gaz obtenu de l'huile était environ trois fois celui du gaz du charbon, et de plus, que chaque heure consume environ quatre fois plus de gaz de charbon que de gaz huileux. On emploie maintenant les huiles de baleine, de colza, etc., et même les semences oléagineuses pour l'extraction du gaz olifiant, et on le purifie, comme nous l'avons dit, en lui faisant traverser de la chaux suspendue ou délayée dans l'eau[8]. »
L'avantage principal du gaz d'huile, par rapport au gaz de houille est l'absence de sulfure d'hydrogène nécessitant une épuration chez ce dernier. Par contre la combustion du gaz d'huile consomme deux fois plus d'oxygène que le gaz de houille[9].
Autre désavantage sur le gaz de houille, la distillation de la houille produit du coke, dont la vente à elle seule couvre le prix d’achat de la houille. La distillation de l'huile ne produit aucun produit comparable.
Le gaz d'huile seul sera exploité avec plus ou moins de succès avant d'être remplacé par le gaz de houille, plus intéressant économiquement.
Fresnel s'y intéressa[10] et certain phares en seront équipés (Exemple: Tourelle de la Plate).
Gaz de résine
Des expériences réalisées à Anvers vers 1837 montrent que le pouvoir éclairant du gaz de résine est deux fois supérieur au gaz de houille
Ainsi, la ville de Gand fut dans un premier temps éclairée au gaz de résine; mais ce gaz ne donnant aucun résidu (la houille donne du coke, qui se vend aussi cher que la houille elle-même, de sorte que le gaz ne coûte presque rien), la compagnie anglaise responsable de l'éclairage à Gand, abandonna le gaz de résine pour le gaz de houille[11].
Gaz de tourbe
Les expériences menées vers 1850 pour obtenir du gaz de tourbe ne furent pas concluantes, le pouvoir éclairant du gaz de tourbe étant trop faible[8].
Gaz à l'eau
Le gaz à l'eau est un gaz de synthèse produit par action de l'eau sur du charbon ou du coke incandescents.
La réaction est la suivante :
- H2O + C = H2 + CO
Dans une usine à Narbonne en 1859:
Autorisée en 1855, l'usine à gaz de Narbonne est installée sur ce qui deviendra la première zone industrielle de la ville, près de l' Eglise Saint-Bonaventure. Symbole du progrès, la voie qui la dessert est appelée rue de l'Avenir (aujourd'hui rue Simon Castan). [12].

A Narbonne c'est le charbon de bois qui est utilisé pour la production du gaz à l'eau.
Les premiers essai de gaz à l'eau mettent en relief la présence de 20 à 21% de monoxyde de carbone, ce qui en fait un gaz toxique et impropre à l'éclairage. Mais en modifiant le procédé (en soustrayant l'acide carbonique avant qu'il ne se transforme en monoxyde carbone) , on obtint plus que 4à 5% de monoxyde carbone, ce qui comparé aux 12% du gaz de houille en fait un gaz très satisfaisant.
La réaction entre la vapeur d'eau se fait dans des cornues en fonte chauffées au rouge-orange. Ces cornues en forme de berceau (1m90x0,39mx0,33m) sont pourvues d'injecteurs pour la vapeur d'eau. L'expérience montre que les fours contenant cinq cornues sont les plus avantageux. La vapeur d'eau est préparée sur le côté dans une chaudière chauffée à la houille et injectée à une pression de 5 à 6 atmosphères. Les injecteurs sont pourvus de capsules de terre réfractaire (80 à 90 par cornue) pour éviter l'obstruction par oxydation du fer au contact de l'eau. Leur disposition font que la vapeur va lécher la surface de charbon de bois incandescent.
Les cornues contiennent de 75 à 80 kilogrammes de charbon de bois. Le chargement des cornues se fait toutes les cinq heures. Le travail de maintenance est moins important que pour le gaz de houille. 1 mètre cube de gaz requiert 324 grammes de charbon de bois et 4791 grammes de houille.
Le gaz obtenu passe dans des réfrigérants et ensuite des épurateurs dont le but est de délester le gaz de l'acide carbonique venu avec l'hydrogène. Cette épuration se fait au moyen de la chaux hydratée placée su des cribles. Pour obtenir 800 mètres cubes d'hydrogène, il faut 1 tonne de chaux vive, ce qui par rapport au gaz de houille est énorme. Pour éteindre cette chaux vive il faut 321 kilogrammes d'eau si bien qu'au final on se retrouve avec 2 tonnes de de [[chaux éteinte: des amas de carbonates de chaux s'accumulent aux abords de l'usine. Ce résidu est vendu pour la confection de mortiers mais est pressentie comme engrais.
Le gaz est stocké dans deux gazomètres en tôle contenant 460 mètres cubes chacun. Les tuyaux dont on s'est servi pour les canalisations sont de en tôle de fer, étamé à l'intérieur, recouverts d'une épaisse couche de bitume imprégné de sable à l'extérieur.
En 1855, Narbonne qui compte 12000 habitants, est éclairée par 214 becs. Chez les particuliers on en trouve 150. Chaque jour sont consommés 650 ou 700 mètres cubes.[13].
Autour de 1885, d'importants agrandissements sont effectués par la Compagnie Générale du Gaz pour la France et l'étranger qui sera nationalisée en 1946 au sein de Gaz de France.
Après la fermeture en 1967, les bâtiments non réutilisables sont détruits[12]
L' acétylène
L'acétylène fût également utilisé à petite échelle dans des applications d'éclairage public. La réaction permettant d'obtenir ce gaz n'est pas une distillation (Ce qui l'exclue des gaz manufacturé si le critère des gaz manufacturés est la distillation), toutefois il se trouva mis en concurrence avec le gaz de houille.
Ainsi la Ville de Callac située dans le département des Côtes-d'Armor et la région Bretagne s’équipe d’un éclairage public à acétylène en 1904. Ce système d'éclairage dura jusqu'à la fin de la Première Guerre mondiale et les années 20 virent l'arrivée de l'éclairage électrique. L’acétylène arrivait un peu tard pour remplacer dans l’éclairage public le gaz de ville dont l’utilisation avait été révolutionnée en 1886 par l’emploi du manchon dû à Carl Auer von Welsbach; si, en 1910, un millier de villes avaient adopté l’acétylène, le développement de l’éclairage électrique allait s’opposer à l’extension de cette utilisation[14].

La lampe à acétylène (ou lampe à carbure) est un moyen d'éclairage le plus souvent portable. Elle a été conçue par le Français Henri Moissan en 1892. La source lumineuse est la flamme de combustion du gaz acétylène, celui-ci résultant de la réaction de l'eau sur le carbure de calcium tous deux contenus dans la lampe.
L'acétylène est un composé chimique hydrocarbure de la classe des alcynes de formule brute C2H2. Il a été découvert par Edmund Davy en Angleterre en 1836. En 1862 l'acétylène peut être synthétisé grâce au chimiste français Marcellin Berthelot qui parvient à fabriquer ce gaz à partir de Carbone et d'hydrogène sous l'action d'un arc électrique. En 1892, le gaz acétylène est produit de manière industrielle grâce au procédé découvert par le pharmacien français Henri Moissan pour fabriquer du carbure de calcium par la fusion du coke et du calcaire à très haute température dans un four à arc électrique. Au canada, un autre chercheur va obtenir les même résultats: Léopold Wilson. Avec l'industrialisation du carbure de calcium en Europe et aux États-Unis, on va pouvoir développer des systèmes d'éclairage autonomes, dés générateurs miniatures qui vont très simplement domestiquer cette réaction entre l'eau et le carbure[15].
Lumière oxhydrique
La lumière oxhydrique dite également lumière Drummond, contemporaine des gaz manufacturés est émise par un bloc de matière réfractaire porté à l'incandescence par la flamme d'un chalumeau oxhydrique (combinaison de l'oxygène et de l'hydrogène). Ce procédé, permettant d'obtenir une lumière très vive a été développé par Goldsworthy Gurney, en 1823[16],[17]. Cette source lumineuse fut ensuite utilisée par un officier de la marine britannique Thomas Drummond, lors d'une mission topographique. Drummond remplaça l'argile utilisée par Gurney par de la chaux afin d'obtenir une lumière encore plus vive[17]. Comme « chaux », se dit « lime » en anglais et « lumière », « light », les anglophones nomment cette lumière « limelight ».
La douceur de la lumière oxhydrique et son bon Indice de rendu de couleur en fait un moyen d'éclairage de choix dans les théâtres et autres lieux de spectacle à partir des années 1830, mais l'on discuta en 1868 de la possibilité de l'utilisation de l'oxygène à la place du gaz de houille comme moyen d'éclairage public. Des expériences furent tentées pour abaisser le coût de production de l'oxygène et une première réalisation concrète sera réalisée sur la place de l'hôtel de ville à l'instigation du barron Haussmann:
La plus importante des qualité de la lumière oxhydrique est « peut-être est sa parfaite innocuité; et, sous ce rapport, on peut dire que sa supériorité sur tous les autres modes d'éclairage en usage est absolue. En effet, cet éclairage, apportant avec lui le gaz combustible et le gaz comburant, n'a pas besoin d'emprunter à l'air ambiant l'oxygène qui est nécessaire à la combustion des autres gaz i il ne vicie donc pas l'air, et dispenserait, pour tous les éclairages intérieurs, de l'emploi des ventilateurs, ventouses, etc., indispensables aujourd'hui[18]. »
L'usage du dioxygène et de l'hydrogène comme gaz d'éclairage implique de dédoubler les canalisations, et l'emploi de régulateurs, pour maintenir exacte, la proportion des deux gaz à la sortie des brûleurs...
Notes et références
- gaz définition du Centre national de ressources textuelles et lexicales sur le site cnrtl.fr
- « TECHNOLOGIE DU BOIS - La composition chimique du bois », inforets.free.fr (consulté le )
- LES DÉBUTS OBSCURS DU GAZ D’ÉCLAIRAGE sur un site consacré à la chimie
- Gérard Sarlos, Pierre-André Haldi, Pierre Verstraete: Systèmes énergétiques: Offre et demande d'énergie : méthodes d'analyse. PPUR presses polytechniques, 2003Livre numérique google
- Michel Raoult, Histoire du chauffage urbain, Éditions L'Harmattan, 2007, p.31.
- Ibrahima Sakho. Guide pratique du lycéen - Chimie Première S. Éditions Publibook 2010Livre numérique google
- Justus Liebig, Gerhardt. Traité de chimie organique 1842 (Livre numérique Google)
- Monbrion (M.) "Dictionnaire universel du commerce, de la banque et des manufactures ...: Par une société de négocians et de manufacturiers " A. Delahays, 1851Livre numérique google
- Bulletin des sciences technologiques. Imprimerie de Fain, 1824 (Livre numérique Google)
- Augustin Fresnel Œuvres complètes d'Augustin Fresnel: "Phares et appareils d'éclairage". Imprimerie impériale, 1870 Livre numérique google
- Académie royale des sciences et belles-lettres de Bruxelles. Mémoires couronnés par l'Académie royale des sciences et belles-lettres de Bruxelles, volume 13 ; volume 1837 (Livre numérique Google)
- Usine à gaz de Narbonne sur wiki-narbonne.fr
- B. Verver L' éclairage au gaz à l'eau à Narbonne et l'éclairage au gaz Leprince examinés et comparés à l'éclairage au gaz de houille ordinaire; F. Renard, 1859 (Livre numérique Google)
- La Ville de Callac s’équipe d’un éclairage public à acétylène en 1904. Sur un site consacré à Callac-de-Bretagne
- Histoire des lampes à carbure sur acethylene.com site dédié à la Lampe à acétylène
- Porter, p. 137
- Lami, p. 525
- Mémoires et compte-rendu des travaux. Société des ingénieurs civils de France.1868. Livre numérique Google