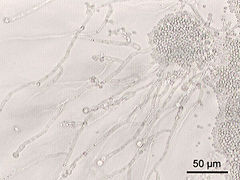
Candida albicans
Candida albicans est l'espèce de levure la plus importante et la plus connue du genre Candida.
| Règne | Fungi |
|---|---|
| Division | Ascomycota |
| Classe | Saccharomycetes |
| Ordre | Saccharomycetales |
| Famille | Saccharomycetaceae |
| Genre | Candida |
Candida albicans est un organisme vivant à l'état naturel dans les muqueuses de l'être humain. On le retrouve dans le tube digestif de 70% des adultes sains[1], et il n'entraîne habituellement aucune maladie ou symptôme en particulier. C'est un organisme commensal saprophyte.
Ce champignon pathogène provoque des infections fongiques (candidiase ou candidose) essentiellement au niveau des muqueuses digestive et gynécologique. Les candidoses sont une cause importante de mortalité chez les patients immunodéprimés comme les patients atteints du sida, les patients cancéreux sous chimiothérapie ou après transplantation de moelle osseuse. Les candidoses orale et œsophagienne sont fréquentes chez le patient atteint du sida. Lorsque Candida s'infiltre dans le flux sanguin, l'infection devient systémique et on parle alors de candidémie (ou candémie). Les candidémies sont caractérisées par une mortalité de l'ordre de 40 %. C. albicans peut donner également une multitude d'autres infections car il s'agit d'un pathogène opportuniste très polyvalent : il peut être responsable d'infection superficielle cutanée, causer un érythème fessier chez les nouveau-nés, une bronchopneumonie et, ou une pneumonie, une vaginite, une balanite ou être responsable d'infections profondes.
Au laboratoire médical, la culture en boîte de Petri des Candida donne des colonies qui sont grandes, rondes, de couleur blanche ou crème (albicans signifie « blanchâtre »).
Cycle de vie
modifier
Le fait que C. albicans soit classé comme étant un champignon asexué peut paraître surprenant, vu sa proximité phylogénétique avec des levures sexuées telles que Saccharomyces cerevisiae. De plus, des gènes impliqués dans le mating (en) et la méiose chez S. cerevisiae ont des orthologues chez C. albicans. La reproduction de C. albicans est majoritairement clonale, avec des échanges génétiques limités entre individus. Pourtant, la découverte de gènes de mating laisse à penser que C. albicans a gardé la capacité de se reproduire et de se recombiner. Ces gènes de mating, appelés MTL (mating type-like), possèdent de grandes similitudes avec les gènes MAT rencontrés chez S. cerevisiae, avec la différence notable que C. albicans possède 4 gènes MTL et non 3 comme c'est le cas chez S. cerevisiae. La plupart des souches de C. albicans sont hétérozygotes pour ces locus et seules 3 à 7 % des souches rencontrées dans la nature sont homozygotes. À l'inverse de S. cerevisiae, pour lesquelles toutes les cellules sont compétentes, seules les souches de C. albicans ayant subi un switch phénotypique de blanc à opaque sont compétentes. Il y a 2 connexions majeures entre le système de mating et la conversion blanc-opaque : 1- c'est le locus MTL qui régule la faculté de C. albicans à effectuer le switch et 2- le mating des cellules en phase opaque est environ 10^6 fois plus efficace que celui des cellules en phase blanche. L'intérêt pour C. albicans de lier les 2 systèmes est peut-être de faire en sorte que les individus ne puissent se recombiner que dans des niches spécifiques. En effet, les cellules en phase opaque sont plus fragiles que les cellules en phase blanche et elles sont instables[2].
Le mating de deux cellules de C. albicans a pour résultat final une cellule tétraploïde, qui doit perdre certains de ses chromosomes pour rétablir la diploïdie.Chez la plupart des champignons, ce processus se fait grâce à une méiose qui complète ainsi un cycle sexuel. Toutefois, chez C. albicans, seul un cycle parasexuel a pu être identifié in vitro, un cycle impliquant une perte coordonnée des chromosomes surnuméraires au fil des divisions cellulaires[3]. Il reste toutefois possible que C. albicans puisse subir une méiose, puisque l'étude de son génome a permis d'identifier plusieurs orthologues de gènes impliqués dans ce processus chez d'autres levures : le locus MTL, NDT80, etc.[4] D'un autre côté, plusieurs gènes importants pour la méiose semblent manquer dans le génome de C. albicans, ce qui suggère que si la méiose peut avoir lieu dans cette levure, son déroulement doit être différent de celui des autres champignons.
Génome
modifier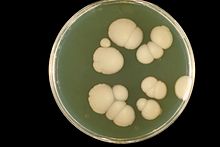
C. albicans est un organisme diploïde qui possède huit paires de chromosomes, le plus grand étant appelé R, les suivants étant numérotés de 1 à 7 selon une taille décroissante. Son génome correspond approximativement à 16 Mb (haploïde) et code environ 6 400 gènes. Le code génétique de C. albicans possède une particularité. Le codon CUG code une sérine et non pour une leucine. Une des caractéristiques de C. albicans est sa très grande hétérozygotie naturelle, ce qui lui confère une grande capacité d'adaptation. Cette hétérozygotie accrue repose sur un réarrangement chromosomique (polymorphisme de longueur du chromosome), mais aussi des translocations réciproques, un polymorphisme nucléotidique ou encore des délétions de nucléotides. Ces modifications du caryotype entraîne des modifications à l'échelle phénotypique, ce qui peut ainsi se traduire par une grande adaptabilité de C. albicans.[5]
Critère d'identification
modifierIl existe plusieurs techniques qui permettent d'identifier C. albicans en laboratoire, par exemple :
- le test de germination positif ; en effet C. albicans formera un hyphe sans constriction une fois placé dans du plasma de lapin à 37 degrés Celsius ;
- le test de chlamydospore sera positif sur milieu RAT dû à la présence de tween ;
- test de l'uréase négatif sur milieu Christensen ;
- colonie blanc crème, luisant et crémeuse sur gélose sang ou sabouraud.
Facteurs de virulence
modifier
Un facteur de virulence permet à un pathogène de se maintenir et de proliférer dans son hôte. Il peut alors créer des lésions pathologiques.
Dimorphisme
modifierLe dimorphisme correspond à la transition de la forme levure ellipsoïdale, qui se sépare des cellules filles après la cytokinèse, à la forme hyphale, dont les cellules filles restent liées les unes aux autres par des septa et dont la croissance est apicale. Cette transition morphologique réversible de forme levure à forme champignon[6] peut être induite par un grand nombre de stimuli : le pH, la température, la composition du milieu... Les voies de signalisation conduisant à la filamentation chez C. albicans sont soit MAP-kinase dépendante, soit pH-dépendante, soit AMPc-dépendante. Ces voies sont redondantes : le blocage de l'une d'elles ne suffit pas à inhiber la filamentation. D'autre part, les gènes régulés par ces voies (HWP1, ALS, SAP) sont connus pour leur rôle dans la virulence. Entre les formes levure et hyphale, on peut encore trouver d'autres formes morphologiques comme le pseudohyphe et la chlamydospore, qui sont toutefois plus rares[7].
Adhésines
modifierC. albicans possède un grand nombre de récepteurs à sa surface qui lui permettent de reconnaître les cellules de son hôte et de s'y attacher solidement. Le β-1,2-phosphomannoside se lie ainsi à la galectine via une liaison lectinique. Les protéines de la famille ALS (agglutinin-like sequence) se lient à diverses protéines (laminine, collagène, fibrinogène) ainsi qu'à des cellules épithéliales et endothéliales via des liaisons non covalentes[8]. Enfin, la protéine Hwp1p (hyphal wall protein) se lie à son substrat de manière covalente par l'action d'une transglutaminase.
Enzymes sécrétées
modifierC. albicans possède toute une gamme d'enzymes hydrolytiques qui sont exprimées différentiellement selon l'environnement. On peut citer par exemple les enzymes de la famille SAP (secreted aspartyl proteinase), qui compte actuellement 10 membres et dont les rôles sont variés (dégradation de protéines, dégradation des structures cellulaires et tissulaires de l'hôte, dégradation du système immunitaire). Leur expression dépend du pH, de la localisation de C. albicans et de sa forme morphologique[9]. C. albicans possède encore des phospholipases (A, B, C et D) et des lipases (1 à 10).
Traitements utilisés contre C. albicans
modifierLes antifongiques utilisés actuellement ont de nombreuses cibles : la paroi cellulaire, la membrane plasmique, la synthèse de l'ergostérol, l'ADN, l'ARN... Ces antifongiques sont soit fongistatiques, soit fongicides.
Polyènes
modifierLes polyènes (ex. : Amphotéricine B [AmB], nystatine) sont des antifongiques naturels à action fongicide. L'AmB se lie à l'ergostérol de la membrane du champignon et crée des pores, augmentant ainsi la perméabilité de la membrane. Des composés essentiels à la vie du champignon diffusent ainsi hors du cytosol (ions K+...) ce qui conduit à la mort de l'organisme.
L'AmB connaît une réactivité croisée avec le cholestérol, le stérol principal chez l'homme. L'AmB peut donc être toxique à haute dose.
Analogues de pyrimidine
modifierLes analogues de pyrimidine (ex. : 5-fluorocytosine [5-FC]) sont des antifongiques à action fongicide. La 5-FC pénètre la cellule fongique et inhibe la synthèse d'ARN et d'ADN. Les analogues de pyrimidine n'affectent pas l'homme, car la cytosine déaminase n'existe pas dans les cellules ou y est faiblement active.
Azoles
modifierLes azoles forment la classe la plus répandue d'antifongiques à action fongistatique. On les classe en 2 sous-familles : les imidazoles (kétoconazole, miconazole) et les triazoles, plus récents (fluconazole, voriconazole, itraconazole). Les azoles inhibent l'action du gène ERG11 impliqué dans la biosynthèse de l'ergostérol. La membrane est ainsi fragilisée et le champignon ne peut plus croître. Le gène ERG5 est une cible secondaire des azoles.
Allylamines
modifierLes allylamines (ex. : terbinafine, naftinine) sont des antifongiques à action fongistatique qui inhibent la fonction de l'enzyme codée par ERG1, une squalène epoxidase. L'effet fongistatique est le résultat de la déplétion en ergostérol et de l'accumulation de stérols toxiques dans la cellule.
Morpholines
modifierLes morpholines (ex. : amorolfine) ont une activité fongistatique en inhibant la fonction de 2 enzymes impliquées dans la biosynthèse de l'ergostérol : la C-14 stérol réductase (codée par ERG24) et la C-8 stérol isomérase (codée par ERG2).
Echinocandines
modifierLa paroi cellulaire a une fonction importante chez les champignons. C'est pourquoi de nouveaux antifongiques ont été développés, qui ciblent la synthèse des éléments de ladite paroi. Les échinocandines ciblent par exemple le produit du gène FKS1 de C. albicans, qui code une β-1,3-glucane synthase. Les échinocandines (ex. : caspofongine, micafongine...) ont une forte activité fongicide et ne présentent pas de réactivité croisée avec d'autres antifongiques[10],[11],[12],[13],[14].
Autres types d'antifongiques chimiques
modifierParmi les autres types d'antifongiques, plus ou moins récents, on retrouve les sordarines, qui ciblent la synthèse de protéines (inhibiteurs du facteur d'élongation 2), l'auréobasidine A (inhibiteur de la synthèse de céramides), les inhibiteurs de pompes à protons ou des transporteurs ABC, etc.
La Ciclopiroxolamine fait partie de la famille des pyridones (dictionnaire Vidal 1996) et les candidoses cutanées font partie de ses indications thérapeutiques.
Antifongique naturel
modifierL'Horopito (Pseudowintera colorata), une plante qui pousse en Nouvelle-Zélande, est un antifongique naturel qui a une puissante action contre le C. albicans[10],[11],[12],[13],[14]. Cette plante est par ailleurs 32 fois plus efficace lorsqu'elle est associée à l'anis épicé d'Amérique du Sud (Pimpinella anisum)[15]. L'huile essentielle d'arbre à thé est également connue pour son efficacité contre Candida[16].
Les extraits de romarin (Rosmarinus officinalis) et de rhizome de gingembre (Zingiber officinale) sont aussi très efficaces contre toutes les souches de Candida courantes chez l'homme et ont été testés in vitro ainsi qu'in vivo chez la souris C57BL6. L'extrait éthanolique de gingembre est même plus efficace que le fluconazole sur Candida albicans, sa CMI (concentration minimale inhibitrice) est plus faible que l'antifongique le plus souvent administré pour traiter les candidoses gynécologiques[17].
Phénomènes de résistance
modifierRésistance aux analogues de pyrimidine
modifierCertaines souches de C. albicans peuvent développer une résistance à la 5-FC en exprimant des formes mutées de cytosine perméase ou de cytosine déaminase. Mais la majorité des souches présentent des mutations dans le gène FUR1 qui code une phosphoribosyltransférase, empêchant ainsi à la 5-FC de s'intégrer dans l'ARNm lors de sa synthèse.
Résistance aux azoles
modifierLa résistance aux azoles est un phénomène courant chez C. albicans. Il intervient généralement lors de traitements prolongés avec le même médicament. La résistance peut intervenir de 4 manières[18] :
- Surexpression de la cible : la cible des azoles, la 14α-lanostérol déméthylase, peut être surexprimée dans la souche de manière que les molécules d'azoles ne soient jamais assez nombreuses pour inhiber toutes les enzymes présentes. La synthèse de l'ergostérol peut ainsi se poursuivre normalement
- Altération de la cible : le gène ERG11 peut être muté de manière à ne plus coder qu'une forme modifiée de la 14α-lanostérol déméthylase, dont l'affinité pour les azoles est nettement diminuée. On a actuellement recensé plus de 18 mutations différentes, regroupées dans 3 hot spots différents, qui représentent soit le site d'entrée du substrat ou de l'azole, soit le site de liaison du subtrat/azole, soit l'hème.
- Efflux des azoles : les azoles peuvent être expulsés hors de la cellule par la surexpression de transporteurs multidrogues. De cette manière, les azoles ne sont jamais assez concentrés dans la cellule pour réussir l'inhibition d'Erg11p. Deux familles de transporteurs sont impliquées dans ce phénomène : la famille des Major Facilitators (ex. : CaMDR1) et la famille des ATP-binding cassette transporteurs (transporteurs ABC) (ex. : CDR1 et CDR2). La surexpression de cette dernière famille de transporteurs peut intervenir lorsque le facteur de transcription TAC1 est muté.
- Absence d'intermédiaire toxique : lorsque la 14α-lanostérol déméthylase est inhibée, il y a accumulation dans la cellule d'un intermédiaire méthylé, le 14α-méthylfécostérol. Ce composé est pris comme substrat par l'enzyme Δ5-6 désaturase codée par ERG3 pour former le 14α-méthyl-ergosta-8,24(28)-dien-3β, 6α-diol, un composé toxique. Des souches ont été trouvées qui possèdent des allèles ERG3 déficients. Ces souches ne transforment donc pas les composés méthylés en composés toxiques, ce qui explique leur résistance aux azoles.
Cette absence d'Erg3p est couplée généralement à une résistance à l'AmB, puisque l'absence de la Δ5-6 désaturase coupe la voie de biosynthèse de l'ergostérol.
Résistance aux échinocandines
modifierLes phénomènes de résistance aux échinocandines restent rares. On sait toutefois qu'une mutation dans le gène FKS1 suffit à rendre la souche résistante à l'action des échinocandines.
Notes et références
modifier- (en) Askin Erdogan et Satish S. C. Rao, « Small Intestinal Fungal Overgrowth », Current Gastroenterology Reports, vol. 17, no 4, , p. 16 (ISSN 1522-8037 et 1534-312X, DOI 10.1007/s11894-015-0436-2, lire en ligne, consulté le )
- (en) Bennett, R.J. et A.D. Johnson, « Mating in Candida albicans and the search for a sexual cycle », Annu rev Microbiol., no 59, , p. 233-255
- (en) Bennett, R.J. and A.D. Johnson. 2003. « Completion of a parasexual cycle in Candida albicans by induced chromosome loss in tetraploid strains » Embo J. 22: 2505-2515
- (en) Tzung K.W. et al. 2001. « Genomic evidence for a complete sexual cycle in Candida albicans » Proc Natl Acad Sci USA 98: 3249-3253
- (en) T. Jones, N. A. Federspiel, H. Chibana et J. Dungan, « The diploid genome sequence of Candida albicans », Proceedings of the National Academy of Sciences, vol. 101, no 19, , p. 7329–7334 (ISSN 0027-8424 et 1091-6490, PMID 15123810, PMCID PMC409918, DOI 10.1073/pnas.0401648101, lire en ligne, consulté le )
- (en) David Kadosh, « Regulatory mechanisms controlling morphology and pathogenesis in Candida albicans », Current Opinion in Microbiology, vol. 52, , p. 27–34 (PMID 31129557, PMCID PMC6874724, DOI 10.1016/j.mib.2019.04.005, lire en ligne, consulté le )
- (en) Sudbery P, N. Gow and J. Berman. 2004. Trends in microbiology
- (en) Sheppard DC. et al. « Functional and structural diversity in the Als protein family of Candida albicans » J Biol Chem. 2004;279: 30480-9.
- (en) Borg-von Zepelin, M., S. Beggah, K. Boggian, D. Sanglard and M. Monod. 1998. « The expression of the secreted aspartyl proteinases Sap4 to Sap6 from Candida albicans in murine macrophages » Mol Microbiol. 28: 543-554
- Laverdière, M. et al. 2006. « Progressive loss of echinocandin activity following prolonged use for treatment of Candida albicans oesophagitis » J Antimicrob Chemother. 57:705-708
- (en) « Antibiotic substances from New Zealand plants II. Polygodial, an anti-Candida agent from Pseudowintera colorata » McCallion, R.F., Cole, A.L.J, Walker, J.R.L., Blunt, J.W. and Munro, H.G., 1982, Planta Medica 44, p. 34-138.
- (en) « Polygodial, an antifungal potentiator » Kubo, I. & Taniguchi, M., 1988, Journal of Natural Products 51 (1), p. 22-29.
- (en) « In vitro antifungal susceptibilities of Candida albicans and other fungal pathogens to polygodial, a sesquiterpene dialdehyde » Lee, S.H., Lee, J.R., Lunde, C.S. & Kubo, I., 1999, Planta Medica 65, p. 204-208.
- (en) « Fungicidal activity of polygodial in combination with anethole and indole against Candida albicans » Himejima, M. & Kubo, I. 1993, J. Agric. Food Chem., 41, p. 1776-1779.
- (en) « Anethole, a synergist of polygodial against filamentous microorganisms » Isao Kubo, Masaki Himejima. Université de Californie.
- (en) « In vitro and in vivo activity of melaleuca alternifolia mixed with tissue conditioner on Candida albicans », Oral Surgery, Oral Medicine, Oral Pathology, Oral Radiology and Endodontics, (DOI 10.1016/j.tripleo.2007.08.025).
- S. Akroum, « Activité antimicrobienne des extraits de Rosmarinus officinalis et Zingiber officinale sur les espèces du genre Candida et sur Streptococcus pneumoniae », Annales Pharmaceutiques Françaises, vol. 79, no 1, , p. 62–69 (ISSN 0003-4509, DOI 10.1016/j.pharma.2020.06.003, lire en ligne, consulté le )
- (en) White, T.C., K.A. Marr, and R.A. Bowden. 1998. « Clinical, cellular, and molecular factors that contribute to antifungal drug resistance » Clin Microbiol Rev. 11:382-402